CONCEPTOS CLAVES:
PH:
- Representa cantidad de protones libres circulando en sangre
- Mas acido más protones
- Menos acido menos protones circulando
- Esto solo es una manera simple de ver la gasometría arterial
- El pH sanguíneo refleja el equilibrio entre la producción y eliminación de ácidos en el cuerpo, siendo esencial para mantener la homeostasis
- El modelo de Stewart enfatiza que este equilibrio no es sólo un reflejo del bicarbonato y el CO2, sino del conjunto de todos los iones en juego y las interacciones químicas en el cuerpo
SIG: (Strong ion GAP)
- Explica mejor el estado ácido base
- Concentraciones de aniones no son medidos (Cetoacidos, glicoles, AAS, hierro, alcoholes)
- Exceso de bases (BE) NO explicado
- Cálculo SIG: BE – (SID – 38) – 2.5 x (4.2 – Albúmina) + Láctico
SID: (Strong ion difference)
- NA+ – CL-
- 38 SID normal sanguíneo (constante fija)
- > 38 alcalotico
- < 38 acidótico
- Condiciona como debo mantener su equilibrio por medio de modificar los demás componentes
- Na+: generalmente NO disociado y es el principal en los positivos, > 90% de los positivos Cl-: 2/3 de las cargas negativas
- El espacio que queda entre el Na y el Cl- (la diferencia de los positivos y los negativos) -> SID
- Cálculo: SID – 38
ANION GAP
- DIFERENCIA ENTRE CATIONES vs. LOS ANIONES: siempre tenderá a la electroneutralidad
- Valor Normal: 12.5 (Este valor de normalidad viene de; albúmina normal (4.2 x 2.5) + ac. láctico aprox. 1 + fosfato aprox. 1) = (4.2 x 2.5) + 1 + 1 : 12.5
- Cómo calcularlo: Na+ – (CL- + HCO3) -> NORMAL 12 (se mantiene estable).
- Elevado hay un ácido culpable (o anión no medido elevado)
- Normal y pH ácido, probable culpable es el Cl- (pero pensar en otras causas: Salicilatos? Urea? )
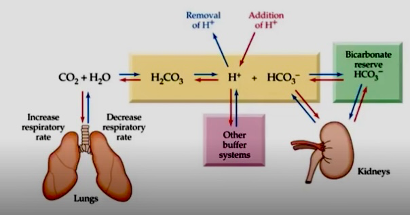
La imagen demuestra la regulación ácido-base según el modelo de Stewart, destacando el papel de los pulmones y los riñones. El equilibrio entre la producción de ácido (H+) y su eliminación es clave. Los pulmones modulan el CO2, que junto con el agua forma ácido carbónico (H2CO3), descomponiéndose en H+ y bicarbonato (HCO3-). Los riñones ajustan la reserva de bicarbonato para compensar cambios en la acidez. Así, el cuerpo mantiene el pH estable mediante un delicado equilibrio entre la eliminación de H+ y la regulación del bicarbonato, influenciado tanto por la respiración como por la función renal.

Esta gráfica compara la distribución de cationes y aniones en una situación de referencia (A) frente a un ejemplo de desequilibrio ácido-base (B) según el modelo de Stewart. En el panel A, el equilibrio entre cationes (principalmente sodio) y aniones (cloruro, bicarbonato, albúmina) se mantiene, reflejando un estado ácido-base normal. En el panel B, se observa una alteración en la proporción de aniones, destacando un aumento en lactato y otros aniones no medidos, lo que resulta en un desequilibrio que puede explicar un anion gap elevado y acidosis metabólica. Este cambio ilustra cómo los desequilibrios en los iones fuertes y aniones no medidos pueden alterar el equilibrio ácido-base, subrayando la utilidad del modelo de Stewart para interpretar estas alteraciones.
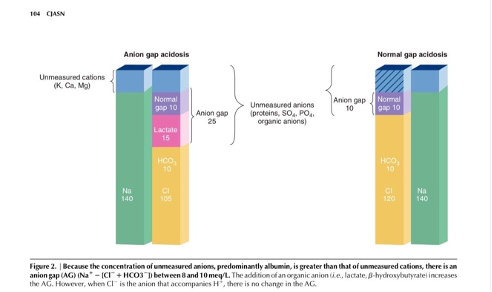
La gráfica compara la acidosis metabólica con anion gap elevado y la acidosis con anion gap normal en términos del modelo de Stewart. En la acidosis con anion gap elevado, la acumulación de aniones no medidos, como lactato y otros ácidos orgánicos, desplaza el bicarbonato (HCO3-), lo que resulta en un aumento del anion gap. Esto sugiere una acumulación de ácidos que no son compensados por los mecanismos normales, como el intercambio de cloruro (Cl-) o el equilibrio de otros iones fuertes. En contraste, en la acidosis con anion gap normal, la pérdida de bicarbonato se compensa directamente con un aumento en cloruro, manteniendo el anion gap estable. Esta distinción es crucial para diferenciar entre las causas de acidosis metabólica y guiar el manejo terapéutico adecuado.
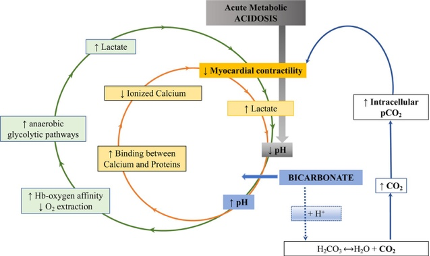
La imagen representa las interacciones complejas en la acidosis metabólica aguda según el modelo de Stewart. A medida que aumenta el lactato, disminuye el pH, lo que afecta la contractilidad miocárdica y el equilibrio del calcio ionizado. La acidosis favorece las vías glucolíticas anaeróbicas, lo que eleva aún más el lactato. La disminución del pH también incrementa el CO2 intracelular, lo que activa el sistema de bicarbonato como amortiguador, tratando de neutralizar el exceso de H+. Este ciclo de compensaciones refleja cómo la acidosis metabólica altera múltiples sistemas fisiológicos, resaltando la necesidad de un manejo cuidadoso en situaciones críticas.
GAP Osmolar
- Osmol medida – (2Na+ Glu/18 + BUN/2.8).
- VN: 275-295 mOsm/kg.
- Principalmente determinado por la natremia.
ALBÚMINA
- Constante fija de albúmina 4.2
- > 4.2 acidótico
- < 4.2 alcalotico
- Se ajusta x 2.5
- Cálculo: 2.5 x (4.2 – albúmina medida)
- Si no se cuenta con reporte, evaluar paciente, género, peso, edad, si luce normal, su valor será cero (0), si paciente emaciado, pequeño, VEC elevado, será +2
- NO pasa al Extravascular
- Valor Normal: 3.5 – 4.5
ÁCIDO LÁCTICO
- El medido o el faltante según todo lo demás esté explicado
BE
- Debe ser cero (0) +/- 2
- Buscar que lo explica?
- SID?
- Lactico?
- Albumina?
- Aniones no medidos? (ANM)
- Cuerpos cetonicos
- Acoholes
- Salicilatos
- Medicamentos (isoniazida, hierro)
ENFRENTAMIENTO CLASICO
- Características del paciente
- Trastorno primario
- Trastorno secundario
- Compensación?
- GAP Iónico
- GAP Osmolar
«Caso Clínico: Enfoque Integrado»
- Hombre, 26 años
- Deserción escolar
- Vive con su madre
Antecedentes: Dm 2 IR
Tratamiento: mala adherencia a terapia.
- Fcos: Insulina ultrarapida y Toujeo (No aporta dosis), ayer no se las administra.
Tóxicos:
- Tabaquismo activo hace algunos años, policonsumo (se desconoce a que?) y consumidor habitual de OH.
Anamnesis:
Cuadro clínico de 1 día de evolución, inicia nauseas, vómitos, dolor abdominal superior, escasos episodios de diarrea
Llevado a SU porque ¨ Lo ven muy mal¨
Evaluación primaria:
Pasar a reanimador, Monitor, VVP, O2
A: VA Estigmas de vómitos en la boca
- Aspirar secreciones, permeabilizar VA, columna cervical en linea media, no sugiere lesiones
B: FR 36x´, SaO2: 90% (21%), con esfuerzo respiratorio
- MNR 100% a 15 LXM
C: PA 90/42, pam:58mmHg, FC 132, extremidades frías, hipoperfundido, llenado capilar 4 sg.
- Critaloides 2000cc Sol.0.9% EV a chorro + SRL 2000cc, evaluar respuesta, si no responde tras reanimación inical con volumen
- DVA 0.1mcg/kg/min. Por VVP (ideal proximal y dosis baja), y evaluar respuesta (definir si se sube o baja dosis segun respuesta)
US: Protocolo RUSH:
- Patron de shock hipovolemico/distributivo
- Corazon hiperdinamico, sin derrame pericardico, VI>VD, VCI colapsada, pulmones deslizamiento pleural bilateral positivo, sin LLA, Ao abdominal <4cm
D: Glasgow 7/15, sopor superficial, pupilas isocoricas, normoreactivas, inatento, moviliza 4 extremidades
- Posicionar cabeza, evaluar funciones corticlaes, si no protege VA, considerar TOT (optimizando lo mejor posible la fisiopatologia del paciente previo a SRI)
E: Sin lesiones en cabeza, ni en extremidades
Completando eval.1ria.
- T° 36.9
- ECG: taquicardia sinusal, pr<0.2, QRS 0.08sg, QTc: 430, sin lesión, ni isquemia miocárdica, aVR sin Q patológica, ni elevación del ST
- HGT: HI
19:20 (GSV Inicial – GEM/Rapid Point)

- Ph: 7.20
- HCO3-: 15.4 mmol/L
- PaCO2: 39.7 mmHg
- PaO2: 52.2 mmHg
- BE -11.9 mmol/L
- Na+: 127mmol/L
- K+: 4.05 mmol/L
- Cl-: 81 mmol/L
- Ca++:4.3mg/dl
- AnionGap: 34.9
- Lactato: 30.9 mg/dl
- Glucosa: ——
- Omolaridad no reportada
- Albúmina: 3.2
INTERPRETACIÓN ACIDO-BASE: # GSV inicial
Cálculo del SID (Strong Ion Difference):
SID = Na+ − Cl− = 127 − 81 = 46 mmol/L
Restar 38 del SID:
SID − 38 = 46 − 38 = 8 mmol/L (No explica nada de la BE, por el contrario hacen falta sumar 8 bases)
Ajuste por albúmina:
Ajuste por Albúmina = 2.5 × (4.2 − 4.2) = 0.0 mmol/L
(No hay ajuste porque la albúmina está en su valor normal de 4.2 g/dL)
Conversión del lactato de mg/dL a mmol/L:
Lactato = 30.9 mg/dL × 0.111 = 3.4299 mmol/L (Explicando parte de la BE -3.4/-11.9)
Aplicación de la fórmula para calcular el SIG:
SIG = BE − (SID − 38) − 2.5 × (4.2 − Albúmina) + Lactato
SIG = -11.9 − 8 − 0.0 + 3.4299 = -16.4701 mmol/L
Resultado Final del SIG:
-16.47 mmol/L
ENFRENTAMIENTO CLASICO
- Características del paciente
- Hipotenso, mala perfusión periférica
- Trastorno primario
- Acidosis Metabólica
- Trastorno secundario
- Compensación:
- Winter para HCO3 15.4 (29-33mmHg esperado)
- PaCO2 medido: 39.7
- No compensada
- GAP Iónico
- Acidosis Metabólica con anion GAP elevado
- GAP Osmolar
- Se mantiene en este momento sin registro de glucosa por HGT, rapid point no lo reporta y aun no se cuenta con glicemia.
- El paciente presenta una acidosis metabólica severa con un anion GAP elevado, no completamente explicada por el SID o el lactato, lo que sugiere la presencia de aniones no medidos, como cuerpos cetónicos o tóxicos. La presencia de un SIG negativo y elevado refuerza el análisis, indicando un desequilibrio ácido-base significativo. La falta de compensación respiratoria adecuada y la hipoperfusión periférica agravan el cuadro clínico. Es esencial continuar la evaluación, incluyendo la medición de la glucosa y el GAP osmolar, para guiar el tratamiento de manera efectiva, enfocándose en identificar y corregir las causas subyacentes del desequilibrio metabólico.
20:20 (GSV Control posterior a intervenciones iniciales)

- Ph: 7.26
- HCO3-: 17.9 mmol/L
- PaCO2: 40.6 mmHg
- PaO2: 46 mmHg
- BE -8.7 mmol/L
- Na+: 134 mmol/L
- K+: 3.6 mmol/L
- Cl-: 95 mmol/L
- Ca++:4.1 mg/dl
- AnionGap: 25.7 mmol/L
- Lactato: 26.9 mg/dl
- Glucosa: ——
- Osmolaridad se mantiene sin reportar
- Albúmina: 3.2
INTERPRETACIÓN ACIDO-BASE: # GSV Control
Cálculo del SID (Strong Ion Difference):
SID = Na+ − Cl− = 134 − 95 = 39 mmol/L
Restar 38 del SID:
SID − 38 = 39 − 38 = 1 mmol/L
Ajuste por albúmina:
Ajuste por Albúmina = 2.5 × (4.2 − 4.2) = 0.0 mmol/L
(No hay ajuste porque la albúmina está en su valor normal de 4.2 g/dL)
Conversión del lactato de mg/dL a mmol/L:
Lactato = 26.9 mg/dL × 0.111 = 2.9859 mmol/L
Aplicación de la fórmula para calcular el SIG:
SIG = BE − (SID − 38) − 2.5 × (4.2 − Albúmina) + Lactato
SIG = -8.7 − 1 − 0.0 + 2.9859 = -6.7141 mmol/L
Resultado Final del SIG:
-6.71 mmol/L
ENFRENTAMIENTO CLASICO
- Características del paciente
- Hipotenso, mala perfusión periférica
- Trastorno primario
- Acidosis Metabólica
- Trastorno secundario
- Compensación:
- Winter para HCO3 17.9 (33-37 mmHg PaCO2 esperado)
- PaCO2 medido: 40.6
- No compensada
- Compensación:
- GAP Iónico
- Acidosis Metabólica con anion GAP elevado
- GAP Osmolar
- Se mantiene en este momento sin registro de glucosa por HGT, rapid point no lo reporta y aun no se cuenta con glicemia.
- El análisis de los gases iniciales y de control muestra una evolución clínica positiva tras el tratamiento. El paciente presentaba inicialmente una acidosis metabólica severa con un anion GAP elevado, no completamente explicada por el SID o el lactato, sugiriendo aniones no medidos como cuerpos cetónicos o tóxicos. La compensación respiratoria inadecuada y la hipoperfusión periférica agravaban el cuadro, reflejado en un SIG negativo significativo.
- En los gases de control, el SID mejora a 39 mmol/L, reduciendo el déficit de bases a 1 mmol/L. Aunque el SIG sigue siendo negativo (-6.71 mmol/L), indicando aniones no medidos persistentes, la mejora del lactato sugiere una respuesta favorable. La PaCO2 de 40.6 mmHg aún indica una compensación incompleta. En resumen, aunque persiste la acidosis con anion GAP elevado, el tratamiento está reduciendo la carga de aniones no medidos y mejorando la función metabólica.
Examen fisico: Completando eval.2ria.
Malas condiciones generales, mucosas muy secas, rr2t, sin ruidos agregados, abdomen blando, distendido, doloroso difuso, sin irritación peritoneal
- Estabilizar y llevar a imágenes
- Cerebro simple. (Enfrentamiento de compromiso de conciencia no traumático, no focaliza)
- Tórax, abdomen y pelvis. (busca de foco descompensante, orientar estudio según sospecha clínica.
- Cobertura antibiótico según sospecha clínica (síntomas que focalizan un sistema)
Análisis y conclusiones clínicas integradas
A pesar de que, a primera vista, los gases iniciales no parecen mostrar una evolución clínica favorable, un análisis detallado de cada punto sugiere una mejoría tanto clínica como gasométrica del paciente. Esto indica que la reanimación está siendo acorde con las condiciones clínicas del paciente. Sin embargo, es importante investigar las causas subyacentes de la descompensación, como infecciones, mala adherencia al tratamiento o consumo de tóxicos, que son factores comunes de descompensación en pacientes diabéticos. En este caso particular, no se trata de un debut diabético ni de una dosis insuficiente de medicación, ya que los familiares reportan una adherencia parcial al tratamiento, además de la asociación con el consumo de tóxicos.
El paciente presenta una acidosis metabólica no compensada tras la primera hora de reanimación, según los dos registros gasométricos (GEM/rapid point). Se observa un anion GAP elevado, donde el ácido láctico no explica completamente el déficit de bases (BE). En este contexto clínico, se interpreta que la acidosis está mayormente explicada por la presencia de aniones no medidos, como los cuerpos cetónicos. El bicarbonato se ha disociado en CO2 y H2O como parte del proceso de compensación de la acidosis inducida por el aumento de hidrogeniones.
Después de la reanimación inicial, los segundos gases venosos muestran una mejoría en el Strong Ion Difference (SID), quedando solo una base por sumar. El anion GAP también se ha reducido, lo que sugiere una tendencia a la mejoría tras una hora de manejo. Esta mejora se manifiesta en la elevación del pH, la mejora del BE, la reducción del anion GAP y la disminución del lactato en más de un 10% durante la primera hora de reanimación. Sin embargo, persiste la dificultad para medir la glucosa, tanto por gasometría como por hemoglutest, lo que impide evaluar correctamente el GAP osmolar. Se presume que este permanece elevado, dado que el hemoglutest sigue registrando niveles altos (HGT en HI).
Estos valores sugieren una mejoría general, lo que justifica la continuación de la terapia. Dado que la potasemia se encuentra en un rango adecuado, es seguro iniciar una bomba de infusión continua (BIC) de insulina sin riesgo de hipocalemia y arritmias ventriculares secundarias a esta, ni hipoglucemia precoz. No obstante, es esencial mantener una vigilancia estrecha durante las primeras fases de la reanimación. En el manejo de la diabetes en este contexto, el objetivo principal no es simplemente reducir la glucosa, sino restablecer la función del sistema metabólico dependiente de la insulina. Esto permite la entrada de glucosa en los tejidos y detiene el mecanismo compensatorio de producción de energía a partir de la beta-oxidación de ácidos grasos, lo que a su vez ayuda a tratar la acidosis y a reducir la producción de aniones no medidos, como los cuerpos cetónicos.
Este análisis debe correlacionarse con la condición clínica del paciente. Aunque la acidosis metabólica persiste sin compensación completa, se observa una tendencia a la corrección del trastorno primario mediante la compensación respiratoria y la disminución del anion GAP. Por lo tanto, si el paciente muestra una mejoría en comparación con el ingreso, con menos esfuerzo respiratorio y alejándose del agotamiento muscular respiratorio, junto con una mejoría en las ventanas macrohemodinámicas (conciencia, presión arterial, y débito urinario) y microhemodinámicas (clínicas: llenado capilar; metabólicas: GSV y lactato), se puede concluir que la reanimación es concordante con el estado clínico del paciente. Esto sugiere que la descompensación metabólica es la causa principal del estado crítico del paciente, descartando, por el momento, otros posibles diferenciales.
Referencias:
- Severinghaus JW. Acid-base balance controversy. Case for standard-base excess as the measure of nonrespiratory acid-base imbalance. J Clin Monit. 1991;7:276–7.
- Stewart PA. Modern quantitative acid-base chemistry. Can J Physiol Pharmacol. 1983;61:1444–61.
- Kellum JA, Elbers PWG. Stewart’s Textbook of Acid-Base. 2nd ed. Barking, UK: Lulu Enterprises UK Ltd.; 2009.
- Story DA, Morimatsu H, Bellomo R. Strong ions, weak acids and base excess: a simplified Fencl-Stewart approach to clinical acid-base disorders. Br J Anaesth. 2004;92:54–60.
- Figge J, Mydosh T, Fencl V. Serum proteins and acid-base equilibria: a follow-up. J Lab Clin Med. 1992;120:713–9.

0 comentarios